Você sabe identificar o Estado de Oxidação dos átomos? Que tal revisar Oxidação e Redução e mandar super bem nas provas do Enem e dos vestibulares? Tem aula do Khan e dicas da professora Munique Dias. Confira abaixo.
Oxidação e Redução, você lembra? E dos macetes ‘Oxi Redox’, você se recorda? – É hora de revisar. Veja agora, começando por dias perguntas bem instigantes: 1 – Você sabe por que o vinho quando exposto ao ar vira vinagre? 2 – Sabe qual a química envolvida por trás dessa transformação? Venha descobrir estas respostas e muito mais com uma super-revisão com vídeo-aulas da Khan Academy e as explicações da professora Munique Dias?
Óxi Redox
Oxidação do Álcool Etílico – O Álcool etílico presente no vinho oxida-se em contato com o oxigênio, isto é, acontece a formação de compostos com maior quantidade de átomos desse elemento.
Os procesos de Oxidação e Redução
– Entenda como os dois processos se relacionam: A oxidação do álcool implica em um processo de transferência de elétrons. Assim, se o álcool etílico sofre a Oxidação, outra espécie deve se reduzir. Efetivamente, ocorre a Redução do oxigênio do ar. Veja na equação da reação.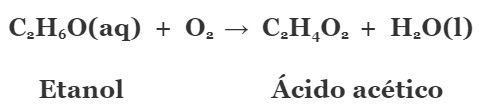 No lado esquerdo estão os reagentes, e no lado direito os produtos resultantes.
No lado esquerdo estão os reagentes, e no lado direito os produtos resultantes.
Entretanto, por não envolver a formação de íons a percepção da transferência de elétrons entre as espécies não é facilmente verificada.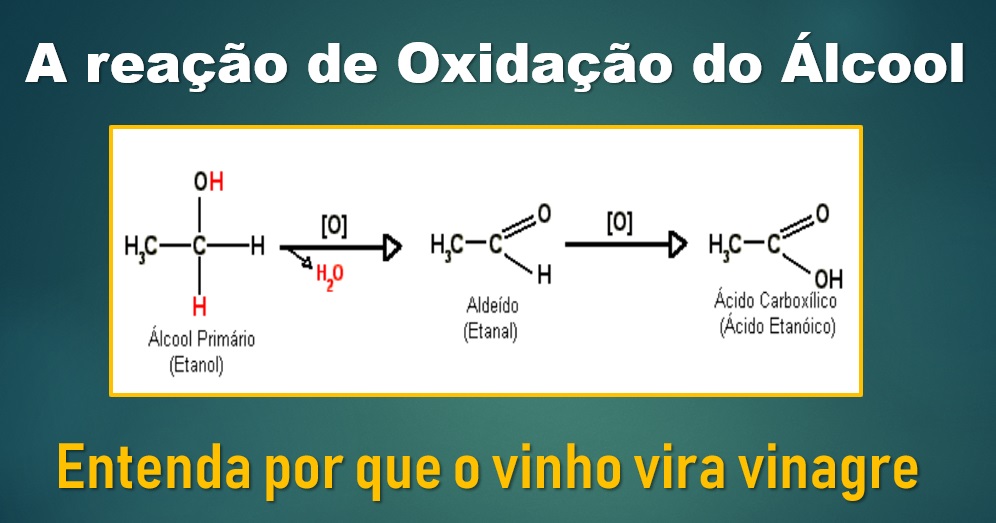 A questão é: Como reconhecer quais substâncias perdem ou ganham elétrons?
A questão é: Como reconhecer quais substâncias perdem ou ganham elétrons?
– A solução para saber quais substâncias perdem ou ganham elétrons está na determinação do numero de oxidação (Nox) dos átomos dos elementos envolvidos no processo.
Entenda o NOX
Número de Oxidação (Nox) – É o número que indica o número de elétrons que um átomo ou íon perde ou ganha para adquirir estabilidade química. Quando o átomo ou o íon perde elétrons, seu Número de Oxidação, o Nox, aumenta, quando ganha elétrons, seu Nox diminui.
Veja na musiquinha da paródia, para não esquecer:
Os professores Sobis e Caio, que dão aulas de Química em Florianópolis (Santa Catarina), prepararam para você uma paródia sobre quem ganha e quem perde elétrons nas reações de Oxidação e Redução.
Gostou do Vídeo? Demais! É bem rápido e super engraçado. Você aprende de uma vez por todas. Confira. O vídeo é do canal Curso Enem Gratuito.
Vamos resumir os estados de oxidação?
Assista agora o vídeo do Curso Enem Gratuito.
É para não esquecer mais! O blog do Enem separou pra você uma tabela com os números de oxidação mais comuns dos principais elementos químicos.
Confira!!
|
Numero de oxidação comum dos principais elementos químicos |
|||||
|
Íons |
Nox |
Íons |
Nox |
Íon |
Nox |
|
Na+ |
+1 |
Fe2+ |
+2 |
F– |
-1 |
|
K+ |
+1 |
Fe3+ |
+3 |
Cl– |
-1 |
|
Mg2+ |
+2 |
Ag+ |
+1 |
Br– |
-1 |
|
Ca2+ |
+2 |
Zn2+ |
+2 |
I– |
-1 |
|
Al3+ |
+3 |
Pb2+ |
+2 |
O2- |
-2 |
|
H+ |
+1 |
Pb4+ |
+4 |
N3- |
-3 |
Vamos deixar o assunto mais interessante? Nesse outro vídeo do Youtube do Curso Enem Gratuito, explicamos com outros exemplos como encontrar o número de oxidação dos átomos.
Você vai ficar fera nesse assunto!
Entenda mais sobre o que é numero de oxidação através da vídeo-aula ministrada pelo professor Henrique Litaiff.
Dica 2 – Faça revisão Enem com Apostilas Gratuitas. O Blog do Enem selecionou para você, para todas as matérias: https://blogdoenem.com.br/category/apostila-enem/
Dica 3 – Veja os vídeos da Khan Academy já traduzidos para o Português pela equipe da Fundação Lemann no http://www.fundacaolemann.org.br/khanportugues/#videos
Exercícios. Tem que fazer para aprender e marcar bem! Que tal praticar um pouco sobre estados de oxidação dos átomos?
Vamos lá!
Determine os números de oxidação para cada elemento das espécies químicas abaixo:
a) HBr
b) ClO4–
c) H2O2
d) NaCl
e) MnBr2
Respostas:
a) HBr
H = +1 ; Br = -1
b) ClO4–
Cl = +7 ; O = -2
c) H2O2
H =+1; O = -1
d) NaCl
Na = +1; Cl = -1
e) MnBr2
Mn = +2; Br = -1