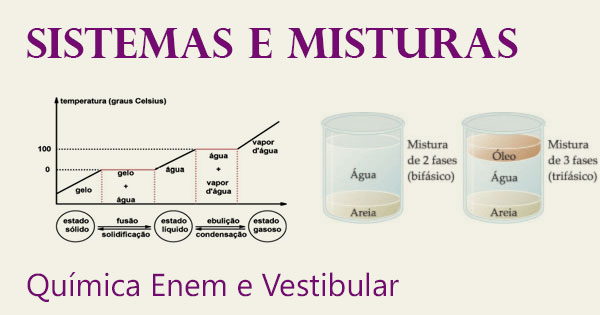
Para garantir sua nota no Exame Nacional do Ensino Médio, revise sobre Misturas, Substâncias Puras e suas classificações nesta aula de Química Enem
Misturas, Substâncias Puras e suas respectivas classificações sempre caem nas provas. Não dá para errar questões fáceis. Veja no resumo gratuito
- Vamos começar pelo básico:
- Elemento Químico: É um conjunto de átomos com mesmo número atômico:
- Exemplos: Ferro (Fe), Hélio (He) e Cloro (Cℓ)
- Os isótopos 1H, 2H e 3H formam o elemento químico hidrogênio.
Substância:
- Substância é todo tipo de matéria que apresenta características próprias.
- Exemplos: água (H2O), gás oxigênio (O2) e ácido sulfúrico (H2SO4).
- Gases, etc.
- Substância simples:
- São aqueles formadas por um único elemento químico.
- Exemplos: Ferro (Fe), gás oxigênio (O2), gás ozônio (O3).
- Substância composta: Formada por dois ou mais elementos químicos.
- Exemplos: Água (H2O), ácido sulfúrico (H2SO4), soda cáustica (NaOH)
- Mistura: É todo tipo de material constituído por duas ou mais substâncias puras, chamadas de componentes da mistura.
- Sistema: É uma porção limitada de matéria que está sendo considerada para estudo.
- Fase: É uma porção homogênea (uniforme de um sistema).
Veja mais sobre as misturas – Resumo do Curso Enem Gratuito
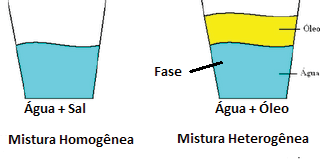
- Sistema homogêneo (monofásico): apresenta um único aspecto e as mesmas características em toda a sua extensão. Pode ser formado por uma ou mais substâncias.
- Exemplos: água, água + sal de cozinha, álcool + gasolina.
- Sistema heterogêneo (polifásico): apresenta diferentes aspectos e diferentes características em sua extensão e é possível distinguir seus componentes. Pode ser formado por uma ou mais substâncias.
- Exemplos: água + óleo, granito (mica, quartzo e feldspato), sal + areia.

Diferença gráfica entre substância pura e mistura
Substância pura: apresenta ponto de fusão e ponto de ebulição definidos.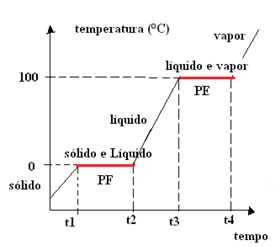
Mistura: apresenta variação na temperatura durante a fusão e a ebulição.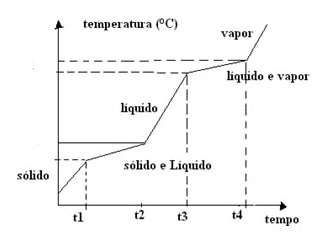
Mistura eutética: apresenta o ponto de fusão em temperatura definida e ponto de ebulição em temperatura variável.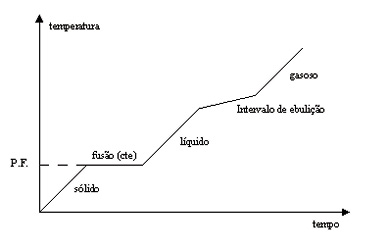
Dica 3 – Revise tudo sobre Química Orgânica, as principais características do carbono e suas classificações em mais uma aula de Química Enem – https://blogdoenem.com.br/quimica-organica-quimica-enem/
Mistura azeotrópica: apresenta o ponto de fusão em temperatura variável e o ponto de ebulição em temperatura definida.
- Alotropia: O mesmo elemento químico forma duas ou mais substâncias simples diferentes:
- Exemplo: Gás oxigênio (O2) e gás ozônio (O3).
Desafios para você resolver e compartilhar a solução
Questão 1
(Enem) De acordo com a legislação brasileira, são tipos de água engarrafada que podem ser vendidos no comércio para o consumo humano:
- água mineral: água que, proveniente de fontes naturais ou captada artificialmente, possui composição química ou propriedades físicas ou físico-químicas específicas, com características que lhe conferem ação medicamentosa;
- água potável de mesa: água que, proveniente de fontes naturais ou captada artificialmente, possui características que a tornam adequada ao consumo humano;
- água purificada adicionada de sais: água produzida artificialmente por meio da adição à água potável de sais de uso permitido, podendo ser gaseificada.
Com base nessas informações, conclui-se que:
a) os três tipos de água descritos na legislação são potáveis.
b) toda água engarrafada vendida no comércio é água mineral.
c) água purificada adicionada de sais é um produto natural encontrado em algumas fontes específicas.
d) a água potável de mesa é adequada para o consumo humano porque apresenta extensa flora bacteriana.
e) a legislação brasileira reconhece que todos os tipos de água têm ação medicamentosa.
Questão 2
Os sistemas a seguir:
- água + álcool hidratdo + óleo
- água + gasolina + álcool
podem ser classificados, respectivamente, como:
a) homogêneo-trifásico e homogêneo-bifásico.
b) heterogêneo-bifásico e heterogêneo-bifásico.
c) homogêneo-monofásico e homogêneo-monofásico.
d) heterogêneo-bifásico e homogêneo-monofásico.
e) homogêneo-monofásico e heterogêneo-bifásico.
Questão 3
No aquecimento de uma amostra de substância pura sólida, obteve-se o seguinte gráfico da temperatura (T) em função do tempo (t).
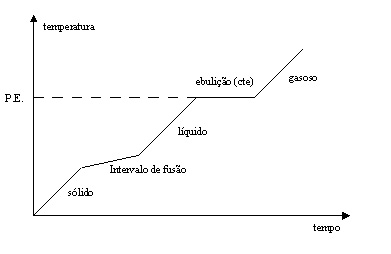
É correto afirmar que:
a) a fusão teve início na temperatura T1.
b) o sólido começou a ser aquecido a partir de 0ºC.
c) à temperatura T2 não existe mais substância sólida.
d) entre o tempo t1 e t2 a substância coexiste em dois estados físicos .
e) a temperatura T3 indica o ponto de fusão do sólido.
Questão 4
(Enem) A água do mar pode ser fonte de materiais utilizados pelo ser humano, como os exemplificados no esquema abaixo.
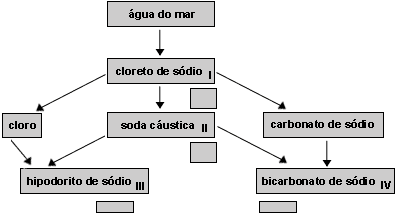
Os materiais I, II, III e IV existem como principal constituinte ativo de produtos de uso rotineiro. A alternativa que associa corretamente água sanitária, fermento em pó e solução fisiológica com os materiais obtidos da água do mar é:
(a) II, III, IV
(b) III, I, IV
(c) III, IV, I
(d) II, III, I
(e) I, IV, III
Questão 5
Considere os sistemas:
I. granito
II. sangue
III. água + gelo
IV. gasolina
V. gás nitrogênio + gás oxigênio
As misturas heterogêneas são:
a) I, II e III.
b) I, III e IV.
c) I e II.
d) II, III e V.
e) I e V.
Você consegue resolver estes exercícios? Então resolva e coloque um comentário no post, logo abaixo, explicando o seu raciocínio e apontando a alternativa correta para cada questão. Quem compartilha a resolução de um exercício ganha em dobro: ensina e aprende ao mesmo tempo. Ensinar é uma das melhores formas de aprender!