Você sabe se é possível controlar o tempo em que ocorre uma reação química? E como explicar que algumas reações ocorrem mais rapidamente do que outras?Tudo isso pode ser entendido através da cinética química, lembra o que é? Que tal relembrar? Com aulas do Khan e dicas da professora Munique Dias.
Olá, o estudo da cinética das reações químicas é muito importante, pois com ele podem-se compreender questões relacionadas ao nosso cotidiano. No entanto, esse assunto não é muito dominado pelos alunos quando aparecem nas provas do Enem e dos vestibulares. Mas com o resumo que o blog do Enem preparou para você, com videoaulas da Khan Academy e as explicações da professora Munique Dias, as questões dessas provas vão ser moleza! Fique com a gente!

Dica: entenda melhor a cinética química com nossas aulas para o Enem
Existem reações muito rápidas como a reação do sódio com a água, reações lentas como o apodrecimento de uma fruta e também reações que demoram anos como a formação do petróleo.

Você deve estar pensando, mas porque essa diferença de comportamento?
Para que as substâncias reajam quimicamente são necessárias duas condições fundamentais:
- Contato entre os reagentes;
- Possibilidade de reação.
Agora, que tal assistir uma super aula sobre cinética química? Veja este vídeo da Khan Academy com o professor Salman Khan:
Dica 2 – Já escolheu a sua profissão? Pense bem antes de entrar em um curso qualquer. Veja aqui a lista das profissões com os 10 piores salários no mercado: https://blogdoenem.com.br/profissao-lista-das-10-piores/
Você lembra-se de alguns conceitos muito importantes para a cinética química como a teoria das colisões, energia de ativação e complexo ativado?Não? Então assista ao vídeo totalmente gratuito de Chemisterman e relembre de forma fácil esses conceitos. https://www.youtube.com/watch?v=FwCsAzpUgT4.
Só para reforçar!
A teoria das colisões: Explica os fatores que influenciam na rapidez das reações. De acordo com essa teoria os aglomerados das substâncias reagentes devem colidir para que a reação química ocorra.
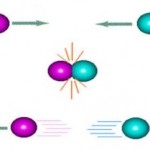
Dica 3 – Quer saber mais sobre a teoria das colisões? Assista a esta vídeo-aula gratuita: https://www.youtube.com/watch?v=FwCsAzpUgT4
A energia de ativação: Energia de ativação (Ea), é a energia mínima que as moléculas devem ter para que a colisão seja favorável e, assim, ocorra a reação.
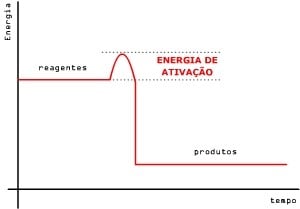
Complexo ativado : É a formação de um intermediário, resultante das colisões, em que todas as partículas das substâncias reagentes estão agregadas, sendo esse intermediário, portanto, muito instável e energético.
Mas como podemos expressar a rapidez de uma reação?
Ela pode ser expressa pela variação de alguma grandeza relacionada com a quantidade de reagente ou produto (concentração, quantidade de matéria, pressão, massa, volume) por unidade de tempo.
Veja:

Entendeu? Não? Então assista a esta vídeo-aula do Descomplica com o professor Carlos Vitorino, e veja mais explicações de como calcular a rapidez de uma reação química e mande super bem nas questões do Enem e dos vestibulares:
A reação de decomposição da amônia gasosa foi realizada em um recipiente fechado:
2 NH3 → N2 + 3 H2
A tabela abaixo indica a variação na concentração de reagente em função do tempo.
| Concentração de NH3 em mol L-1 |
8,0 |
6,0 |
4,0 |
1,0 |
| Tempo em horas |
0 |
1,0 |
2,0 |
3,0 |
Qual é a velocidade média de consumo do reagente nas duas primeiras horas de reação?
Resolução:

Dica 3 – Quer ver outras aulas da Khan Academy? Veja aqui os vídeos Khan Academy já traduzidos para o Português pela equipe da Fundação Lemann no https://www.fundacaolemann.org.br/khanportugues/#videos
Relembrou? Que tal um desafio sobre cinética química?
Numa reação completa de combustão, foi consumido, em 5 minutos, 0,25 mol de metano, que foi transformado em CO2 e H2O. A velocidade da reação será:
Resposta: 0,05 mol/min










