Você lembra da regra “semelhante dissolve semelhante”? Sabe a química que existe por trás disso? Acompanhe no Blog do Enem aulas da Khan e dicas da professora Munique Dias!
Que tal rever um dos assuntos de química que está muito presente em nosso cotidiano e sempre cai nas provas dos vestibulares e do Enem? Aprenda solubilidade das substâncias: ela aparece em várias questões dos vestibulares e do Enem com diferentes enfoques, como por exemplo, inserida nas questões do nosso dia a dia.
Mas, não se preocupe! Com as vídeo-aulas da Khan Academy e as explicações da professora Munique Dias você irá mandar bem nas questões dos vestibulares e do Enem. Acredite!
Alguns princípios básicos da ciência fundamentam as respostas a perguntas simples e cotidianas. Por exemplo, suponha que precisamos remover cera. Como podemos saber qual solvente usar? Uma boa resposta para essa questão seria a regra semelhante dissolve semelhante.
Resumo sobre Ligações Químicas
Para você dominar o tema da Solubilidade a primeira dica é conhecer os fundamentos das Ligações Químicas. É o básico. Veja no resumo com o professor Felipe Sobis, do canal do Curso Enem Gratuito.
Como assim, Semelhante dissolve semelhante?
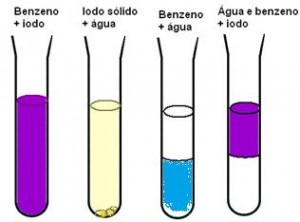
Substâncias apolares como o Iodo, I2, são geralmente mais solúveis em solventes apolares como o benzeno, C6H6, e o tetracloreto de carbono, CCl4, mas pouco solúveis em água, um solvente muito polar.
Benzeno e água são solventes praticamente imiscíveis, por causa da sua diferença de polaridade. Aprenda Solubilidade.
Dica 1: Não lembra o que é polaridade das ligações e das moléculas? Não se preocupe! O blog do Enem da a dica. Assista às vídeo-aulas da professora Larissa Campos, do Curso Enem Gratuito, relembre esse assunto.
Aula 1
Aprenda Solubilidade: Semelhante dissolve semelhante:
Mas o que exatamente é a solubilidade?
A solubilidade é a máxima quantidade possível de um soluto que pode ser dissolvida em certa quantidade de solvente a uma dada temperatura.
Quer saber mais? Aprenda solubilidade agora no vídeo da Khan Academy em que o professor Salman Khan explica sobre a solubilidade. Não deixe de conferir!
Gostou da aula? Então siga as explicações…
Relacionado à solubilidade temos o coeficiente de solubilidade ou grau de solubilidade, que é a quantidade máxima do soluto que pode ser dissolvida em determinado solvente. Mas a solubilidade de qualquer substância depende, entre outras coisas, do tipo de solvente no qual o soluto está disperso.
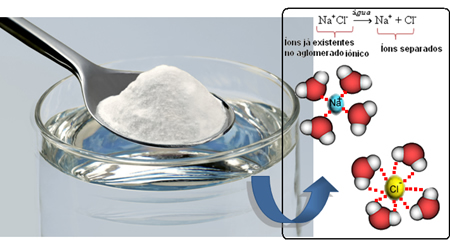
Por exemplo, o NaCl (cloreto de sódio – sal de cozinha) é bem solúvel em água, sendo que em 1 L de água a 20ºC, conseguimos solubilizar até 360 gramas desse sal. Mas, quando o solvente muda para a gasolina, nas mesmas condições de volume, temperatura e pressão, o sal não se dissolve.
Dica 2 – Leia mais sobre o assunto no texto: “Relação entre Força Intermolecular e Solubilidade das Substâncias” – http://brasilescola.com/quimica/forca-intermolecular-solubilidade-das-substancias
Resumo de Forças Intermoleculares
Aprenda Solubilidade com essas dicas:
água é muitas vezes chamada de “solvente universal” porque ela consegue dissolver uma quantidade muito grande de solutos. No entanto, a solubilidade dos materiais em água não ocorre da mesma forma. Veja algumas possibilidades:
- Infinitamente solúveis: O álcool é um exemplo de material que se dissolve na água independente da quantidade adicionada;
- Solúveis: O sal se dissolve na água, mas para cada temperatura ele possui um coeficiente de solubilidade, isto é, uma quantidade máxima de sal que será dissolvida em determinada quantidade de água, chegando ao ponto de saturação. Qualquer quantidade de sal acima desse coeficiente que for adicionada à água, mesmo sob agitação, irá se depositar no fundo do recipiente, sendo chamado de precipitado, corpo de fundo ou corpo de chão;
- Pouco solúveis: São aqueles materiais que se dissolvem em pequena quantidade na água, sendo que a maioria forma um precipitado, como é o caso do café em pó;
- Insolúvel: O ferro não se dissolve em água em nenhuma proporção
No entanto, a água não é o único solvente que existe. Todo material que dissolve outra substância é um solvente. Além disso, uma mesma substância possui diferentes solubilidades em diferentes solventes.
Enquanto o sal é solúvel na água, ele é praticamente insolúvel na acetona ou no acetato de etila (solvente usado para remover esmaltes). Outro exemplo é que o álcool é solúvel tanto na água quanto na gasolina, mas a água e a gasolina não se misturam.
Um exemplo típico do uso da solubilidade dos compostos no nosso cotidiano é o teste da proveta realizado nos postos de gasolina para verificar se a mesma é adulterada ou não.
Mas o que é gasolina adulterada?
É quando se adicionam solventes ou outros compostos à gasolina a fim de tornar o produto mais barato. Geralmente, essa adulteração é feita acrescentando-se etanol à gasolina acima do especificado por lei. Segundo a Portaria 678 de 31/08/2011, do Ministério de Estado da Agricultura, Pecuária e Abastecimento (MAPA), a quantidade adicionada de álcool deve estar entre 20% a 25% em volume.
Dica 3 – Assista ao vídeo do Laboratório Didático Virtual – Escola do futuro-USP – e saiba mais sobre o teste da proveta e como ele é realizado – http://www.labvirtq.fe.usp.br/simulacoes/quimica/sim_qui_gasolinaadulterada.htm












