Certamente você já ouviu falar sobre o buraco na camada de ozônio não é? Agora, é hora de você saber certinho a Reação Química que gera o Ozônio, e o problema do Aquecimento Global.
O que é a camada de Ozônio? – Em volta da Terra há uma frágil camada de um gás chamado ozônio (O3), que protege animais, plantas e seres humanos dos raios ultravioleta emitidos pelo Sol. Na superfície terrestre, o ozônio contribui para agravar a poluição do ar das cidades e a chuva ácida.
Mas, nas alturas da estratosfera (entre 25 e 30 km acima da superfície), é um filtro a favor da vida. Sem ele, os raios ultravioleta poderiam aniquilar todas as formas de vida no planeta.
Na atmosfera, a presença da radiação ultravioleta desencadeia um processo natural que leva à contínua formação e fragmentação do ozônio, como na imagem abaixo: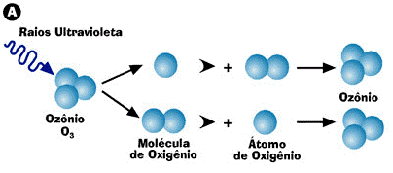
Resumo: A Camada de Ozônio
Veja agora com o professor Raphael Carrieri, do canal do Curso Enem Gratuito, uma introdução perfeita para você dominar o básico sobre A Camada de Ozônio:
A Síntese do professor Carrieri:
- A camada de ozônio é uma camada de gás (O3), situada na estratosfera, que cobre a Terra e impede que diferentes tipos de radiação, principalmente a ultravioleta, entrem na atmosfera.
- Ela vai ser encontrada entre 25 e 30km de altitude. Ela é fundamental aonde ela está, tendo a função de filtrar os rarios ultravioletas. Esses raios são os que causam vários problemas para nós seres humanos, como danos na visão, envelhecimento precoce e câncer de pele. Ou seja: problemão sério!
- As temperaturas na Terra seriam muito elevadas se a gente não tivesse a camada de ozônio para dar uma regulada! ;
- Atualmente existe a dispersão de muitos gases que atuam quimicamente na camada de ozônio dissolvendo-a. É o caso dos CFC’s (Clorofluorocarboneto), Óxido Nítrico (NO)), Ácido Nitroso (HNO₂) e Dióxido de Carbono (CO₂).
- A queima de combustíveis fósseis e outras substâncias tem incrementado esses gases na camada de ozônio gerando um problema sério de dissolver a camada, criando buracos.
- E o principal problema é que a camada de ozônio tem ficado cada vez mais fina na região do Ártico, tendo ali um aquecimento anormal que gela o derretimento de geleiras e, assim, uma mudança nas correntes marítimas.
O que é o Ozônio
O Ozônio é um gás instável, formado por três átomos de oxigênio (forma alotrópica do oxigênio). É um agente oxidante extremamente poderoso, adquirindo características tóxicas em altas concentrações e nas camadas mais baixas da atmosfera.
Na temperatura ambiente ele possui uma cor azul-pálida e em estado líquido possui características explosivas. É produzido na própria estratosfera através de uma reação fotoquímica onde a radiação ultravioleta decompõe o oxigênio em sua forma atômica.
O oxigênio atômico logo em seguida, pela ação de um catalisador, se une a uma molécula de oxigênio originando o ozônio que então sobe para camadas mais altas e sofre novamente a ação dos raios UV que decompõem a molécula de ozônio em uma reação de destruição e criação constante e equilibrada.
O Buraco na Camada de Ozônio
A degradação da camada de ozônio é um dos grandes problemas da atualidade. Esse fenômeno é conhecido como “buraco na camada de ozônio“.
No entanto, não ocorre a formação de buracos e sim a rarefação dessa camada, que fica mais fina, permitindo que uma maior quantidade de raios ultravioleta atinja a Terra.
Em determinadas épocas do ano ocorrem reações químicas na atmosfera, tornando a camada de ozônio mais fina, mas logo ela volta a sua forma original.
Contudo, as atividades humanas têm agravado esse processo, principalmente através das emissões de substâncias químicas halogenadas artificiais, com destaque para os clorofluorcarbonos (CFCs).Essas substâncias reagem com as moléculas de ozônio estratosférico e contribuem para o seu esgotamento.
As Camadas da Atmosfera
Confira agora com o professor Carrieri todas as Camadas da Atmosfera. Assim você aprende mais rápido para saber onde está a Camada de Ozônio.
.
Como os CFCs destroem a camada de ozônio?
Depois de liberados no ar, os CFCs (usados como propelentes em aerossóis, como isolantes em equipamentos de refrigeração e para produzir materiais plásticos) levam cerca de oito anos para chegar à estratosfera onde, atingidos pela radiação ultravioleta, se desintegram e liberam cloro.
Por sua vez, o cloro reage com o ozônio que, consequentemente, é transformado em oxigênio (O2). O problema é que o oxigênio não é capaz de proteger o planeta dos raios ultravioleta. Uma única molécula de CFC pode destruir 100 mil moléculas de ozônio.
A quebra dos gases CFCs é danosa ao processo natural de formação do ozônio. Quando um desses gases (CFCl3) se fragmenta, um átomo de cloro é liberado e reage com o ozônio.
O resultado é a formação de uma molécula de oxigênio e de uma molécula de monóxido de cloro. Mais tarde, depois de uma série de reações, um outro átomo de cloro será liberado e voltará a novamente desencadear a destruição do ozônio.
Em 1987, visando evitar o esgotamento da camada de ozônio, 47 países assinaram um documento chamado Protocolo de Montreal, que passou a vigorar em 1989. Esse Protocolo tem por objetivo reduzir a emissão de substâncias nocivas à camada.
O resultado tem surtido alguns efeitos positivos, visto que vários países pararam de fabricar o gás clorofluorcarbono (CFC), havendo uma queda de aproximadamente 80% no consumo mundial de CFC. No entanto, essa medida não é suficiente para proteger a camada de ozônio.
Relembre outros assuntos de química acessando o nosso blog www.blogdoenem.com.br e gabarite as questões de química nas provas dos vestibulares e do Enem