Substâncias moleculares é um assunto que aparece bastante nas provas do Enem e dos vestibulares de todo o Brasil. Por isso, o Blog do Enem preparou para você um super-resumo para te ajudar a estudar.
A grande variedade de substâncias presentes na natureza se deve à capacidade que os átomos têm de se combinar entre si, e essa propriedade é denominada de Ligação química e pode ocorrer entre os átomos de um mesmo elemento ou de elementos diferentes.
Dica 1– Saiba mais sobre as ligações químicas acessando o Blog do Enem através do link https://blogdoenem.com.br/quimica-enem-ligacoes-quimicas/ e complemente os seus estudos. Não deixe essa dica passar!
A molécula é a menor combinação de átomos que matem a composição da matéria inalterada (os átomos se ligam por ligações químicas covalentes).Os arranjos entre as moléculas formam substâncias moleculares. Nessas substâncias as interações entre as moléculas são muito pequenas, consistindo apenas de forças de Van der Walls (forças intermoleculares).
Que tal ver o exemplo de algumas moléculas?
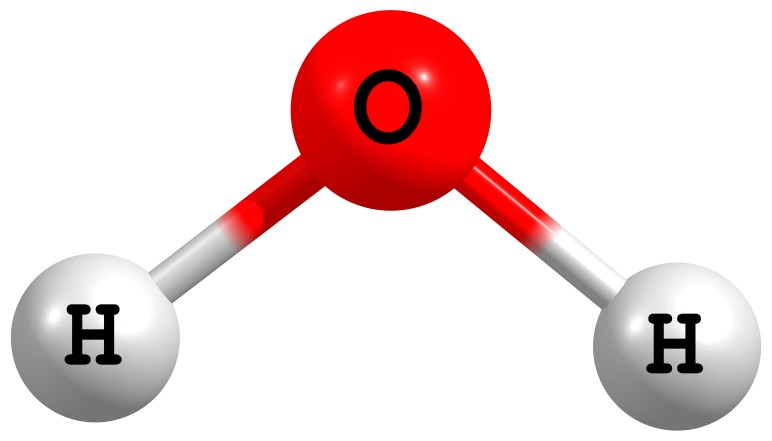
A molécula de água é formada pela ligação entre dois átomos de hidrogênio (H) e um átomo de oxigênio (O). Essa molécula é representada por H2O .
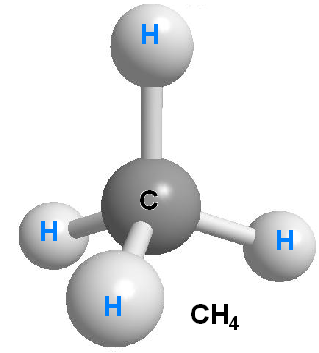
A molécula de metano é formada pela ligação entre um átomo de carbono (C) e quatro átomos de hidrogênio (H).
A água e o metano são substâncias moleculares, pois são formadas por moléculas. Além dessas, podemos citar como exemplos de substâncias moleculares: o açúcar, o álcool e os gases em geral.
Dica 2– O que mais cai em Química nos Vestibulares no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
Não esqueça!
Um composto é molecular quando a sua estrutura apresentar apenas ligações covalentes!
Dica 3 – Que relembrar um poço sobre as ligações químicas? Então acesse o nosso Blog do Enem e estude com a gente! https://blogdoenem.com.br/quimica-enem-ligacoes-quimicas/
Veja um pouco mais sobre o assunto com a videoaula do prof. Sobis sobre forças intermoleculares!
Agora que você já viu o que é uma substância molecular, que tal ver algumas propriedades dessas substâncias?
- Força intermolecular: a temperatura de ebulição (TE) de uma molécula é influenciada pela interação entre seus átomos (forças de atração intermoleculares), quanto mais intensa for a atração entre as moléculas, maior será a temperatura de ebulição.
- Tamanho das moléculas: o tamanho de um composto molecular também influencia no seu ponto de ebulição. Quanto maior for a substância maior será sua superfície de contato, devido ao aumento das interações entre as moléculas, conseqüentemente a temperatura de ebulição irá aumentar.
Dica 4 – Relembre outros assuntos de química acessando o nosso blog www.blogdoenem.com.br e gabarite as questões de química nas provas dos vestibulares e do Enem.

