Vai encarar o próximo Enem ou vestibulares? Então reveja com a gente um assunto bastante cobrado nessas provas que é solução química. Não deixe essa chance passar…
Solução química é uma mistura homogênea entre duas ou mais substâncias. O processo utilizado para obter essa mistura é chamado de dissolução.
Você lembra quais os componentes de uma solução? Vamos rever?
Uma solução é sempre formada pelo soluto e pelo solvente.
Solução = Soluto + Solvente
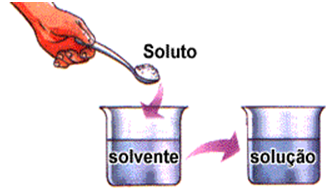
Soluto – substância que será dissolvida.
Solvente – substância que dissolve.
Dica 1 – O que mais cai em Química nos Vestibulares e no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
A água é chamada de solvente universal. Isso porque ela dissolve muitas substâncias e está presente em muitas soluções.
Saiba mais sobre soluções assistindo a uma aula introdutória do Descomplica. Vai deixar essa chance passar?
Agora reveja como são classificadas as soluções! Preste atenção! Cai no Enem e também nos vestibulares de todo Brasil.
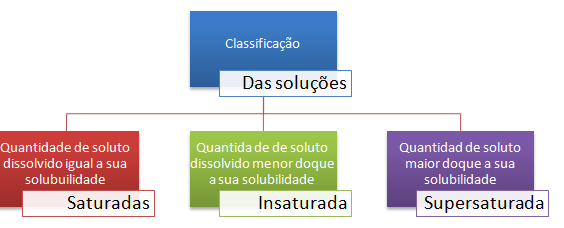
Que tal relembrar sobre a solubilidade das substâncias e mandar ver nas provas dos vestibulares e no próximo Enem? O blog do Enem separou um resumo supercompleto pra você.. Aproveite!
https://blogdoenem.com.br/quimica-solubilidade-aulas-khan-academy/
Dica 2 – Relembre as principais unidades de medidas mais utilizadas nas questões de química dos vestibulares de todo Brasil e no Enem. Acesse o nosso link e veja tudo sobre as unidades e suas conversões. Aproveite essa oportunidade! https://blogdoenem.com.br/unidades-de-medidas-quimica/
Podemos estabelecer diferentes relações entre a quantidade de soluto, de solvente e de solução. Tais relações são denominadas genericamente concentrações.
Usaremos o índice 1 para indicar soluto e o índice 2 para indicar solvente.
Acha difícil decorar fórmulas? Sabendo disso, o blog do Enem preparou para você uma tabela com as relações de concentrações mais utilizadas na química, não deixe de conferir!
|
Nome |
Unidade |
Relação |
Fórmula |
|
Concentração comum ( C ) |
g/L |
Relaciona a massa do soluto em gramas com o volume da solução em litros. |
C = m1/V |
|
Concentração em quantidade de matéria (Cn) |
Mol/L |
Relaciona a quantidade de soluto (mol) com o volume da solução, geralmente em litros |
Cn = n1/V |
|
Título (T) |
Não tem |
Pode relacionar a massa de soluto com a massa da solução ou o volume do soluto com o volume da solução |
T = m1/m e T = V1/V |
|
Densidade da solução (d) |
g/mL ou g/cm3. |
Relaciona a massa e o volume da solução |
d = m/V |
|
As diversas formas de expressar a concentração podem ser relacionadas: C = 1000.d.T |
|||
Dica 3 – Reveja também outro assunto de química que cai bastante nas provas dos vestibulares e do Enem que é Gás Natural. Acesse o nosso blog do Enem e veja um super resumo preparado pela professora Munique Dias. Vai ficar de fora dessa? https://blogdoenem.com.br/quimica-gas-natural/
Saiba mais sobre a concentração das soluções com explicações do conteúdo e exercícios com vídeoaulas totalmente gratuita do professor Rosbergue Lúcio, não fique pra trás! Faça a diferença na hora das provas dos vestibulares e no próximo Enem.









