Massa; Extensão; Divisibilidade; Impenetrabilidade e Compressibilidade estão entre as propriedades gerais da matéria. E tem mais ainda. Veja um resumo completo sobre os tipos de matéria, fenômenos físicos e químicos para mandar bem nas questões de Química do Enem
Revisão online sobre as Propriedades da Matéria. É conteúdo clássico de Química para o Enem e o vestibular. Confira aula gratuita com dicas e exemplos. Vamos começar pelo princípio: Veja o Conceito de Matéria:
Então, para você não esquecer: Matéria é tudo aquilo que possua massa, que ocupe lugar no espaço e que esteja sujeito a inércia. ![]() Ficou mais fácil de captar? – Veja esta outra definição: Matéria é tudo o que tem massa e ocupa espaço. Qualquer coisa que tenha existência física ou real é matéria. Tudo o que existe no universo conhecido manifesta-se como matéria ou energia. A matéria pode ser líquida, sólida ou gasosa. São exemplos de matéria: papel, madeira, ar, água, pedra. Fonte: Portal de Química www.soq.com.br
Ficou mais fácil de captar? – Veja esta outra definição: Matéria é tudo o que tem massa e ocupa espaço. Qualquer coisa que tenha existência física ou real é matéria. Tudo o que existe no universo conhecido manifesta-se como matéria ou energia. A matéria pode ser líquida, sólida ou gasosa. São exemplos de matéria: papel, madeira, ar, água, pedra. Fonte: Portal de Química www.soq.com.br
As Propriedades da Matéria
A lista é bem ampla, e nem todos os tópicos se aplicam universalmente. Alguns tem mais afinidade a uma ou outra manifestação da Matéria. Confira nestes exemplos de Propriedades da Matéria:
- Massa
- Extensão
- Divisibilidade
- Impenetrabilidade
- Compressibilidade
- Elasticidade
- Inércia
Veja agora no detalhe as mais importantes para você mandar bem no Enem
 As propriedades Gerais da Matéria são observadas em qualquer corpo, independente da substância de que ele é feito, são Massa, Extensão, Compressibilidade, Elasticidade, Divisibilidade, Impenetrabilidade, e ainda Propriedades Específicas para alguns corpos tais como ‘odor’, ‘cor’, e muito mais.
As propriedades Gerais da Matéria são observadas em qualquer corpo, independente da substância de que ele é feito, são Massa, Extensão, Compressibilidade, Elasticidade, Divisibilidade, Impenetrabilidade, e ainda Propriedades Específicas para alguns corpos tais como ‘odor’, ‘cor’, e muito mais.
– Recordou? Então, veja abaixo para não esquecer e mergulhar bem no conteúdo.
Massa
Massa é a medida da quantidade de matéria existente em um corpo. A massa mede a resistência que um corpo possui de alterar a situação que se encontra (em repouso ou movimento), ou seja, a inércia. Quanto maior a massa, maior a inércia. Então, Massa é uma das Propriedades Gerais da Matéria!
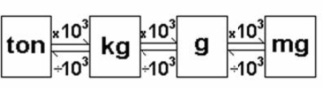
Medida de massa
Extensão:
É o volume que um corpo ocupa no espaço.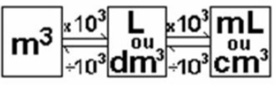
Compressibilidade
É a capacidade que um corpo possui de diminuir seu volume quando uma força é exercida sobre ele. Gases são altamente compressíveis, enquanto líquidos e sólidos praticamente não se comprimem (Exceto sob altíssimas pressões).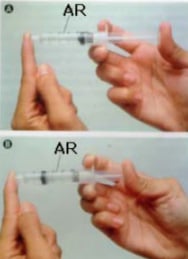 (a) Antes da compressão e (b) após a compressão
(a) Antes da compressão e (b) após a compressão
Elasticidade
É a capacidade que um corpo tem de voltar ao estado inicial após ser submetido a uma força de deformação. Lembrando que essa força deve ser exercida dentro de um limite para não destruir a matéria.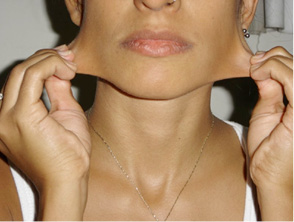 No exemplo, a Elasticidade da pele humana.
No exemplo, a Elasticidade da pele humana.
Divisibilidade
Propriedade que a matéria tem de ser dividida em partículas muito pequenas, sem alterar suas propriedades. Pedreira em funcionamento – as rochas são fragmentadas dando origem às pedras britas, etc. Mas, é a mesma Matéria.
Pedreira em funcionamento – as rochas são fragmentadas dando origem às pedras britas, etc. Mas, é a mesma Matéria.
Impenetrabilidade
Dois corpos não podem estar simultaneamente (ao mesmo tempo) no mesmo lugar no espaço.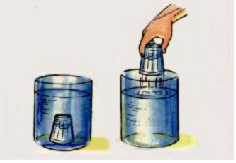 Para que o copo afunde, é necessário que todo o ar presente nele saia. Percebeu como não é nada complicado de aprender as Propriedades Gerais da Matéria?
Para que o copo afunde, é necessário que todo o ar presente nele saia. Percebeu como não é nada complicado de aprender as Propriedades Gerais da Matéria?
Veja agora as Propriedades Específicas da matéria
Aqui no conjunto das propriedades específicas da matéria já é possível identificar um determinado tipo de matéria (substância). Confira nos exemplos:
Organolépticas: são verificadas pelos órgãos dos sentidos: Alguns exemplos: Sabor, odor, cor e textura.
 Uso dos sentidos na percepção das características. Fonte: www.vocesa.com.br
Uso dos sentidos na percepção das características. Fonte: www.vocesa.com.br
Propriedades Químicas: são aquelas relacionadas com as transformações químicas. Alguns exemplos: a queima de um pouco de gasolina e a oxidação de um metal. Fonte da imagem: www.blogspot.com201102sessenta-seculos-e-fogo – combustão do etanol –
Fonte da imagem: www.blogspot.com201102sessenta-seculos-e-fogo – combustão do etanol –
Propriedades Funcionais: são apresentadas por um grupo de substâncias: Alguns exemplos: acidez, basicidade, salinidade.
 Fonte: http://www.educadores.diaadia.pr.gov.br
Fonte: http://www.educadores.diaadia.pr.gov.br
Propriedades Físicas: são aquelas relacionadas com os fenômenos físicos. Essas propriedades podem ser expressas por valores numéricos experimentados e tabelados.  As propriedades Físicas são frequentemente utilizadas para determinar a pureza de certa substância.Fonte: http://vaniateixeira.blogspot.com
As propriedades Físicas são frequentemente utilizadas para determinar a pureza de certa substância.Fonte: http://vaniateixeira.blogspot.com
Alguns exemplos de Propriedades Físicas da Matéria:
- Densidade: é a massa contida por unidade de volume.
- Ponto de fusão: é a temperatura que determinada substância passa do estado sólido para o estado líquido, sob pressão constante.
- Ponto de ebulição: é a temperatura que determinada substância passa do estado líquido para o estado gasoso, sob pressão constante.
- Solubilidade: é a capacidade de uma substância ser miscível em outra. Pode ser quantificada pelo coeficiente de solubilidade.
- Dureza: resistência que um material apresenta de ser riscado.
- Tenacidade: resistência demonstrada por um material de sofrer ruptura pelo impacto.
- Maleabilidade: é a propriedade que um corpo apresenta de ser moldado na forma de lâminas.
Os Fenômenos Químicos e os Fenômenos Físicos
Fenômeno é qualquer transformação que ocorre em um sistema. São divididos em dois tipos: fenômenos químicos e fenômenos físicos.
Fenômeno Químico
Esse tipo de fenômeno altera a natureza dos compostos quem compõem o sistema. Podemos também afirmar que ocorre alteração na estrutura molecular das substâncias desse sistema em transformação.
Exemplos: Combustão do etanol, oxidação de metal, digestão de um alimento, fotossíntese.
Perceba a alteração na estrutura molecular: CaCO3 → CaO + CO2 Combustão – Fonte: www.http://educador.brasilescola.com
Combustão – Fonte: www.http://educador.brasilescola.com
Está valendo pra você? Então mergulhe um pouco mais fundo com essa revisão!
Muito bom este resumo!
Dica 1 – Química Enem: Diagrama de fases. Entenda porque é possível patinar no gelo – https://blogdoenem.com.br/quimica-diagrama-de-fases/
Dica 2 – Química Enem: Fórmula empírica e molecular você sabe como calcular? – https://blogdoenem.com.br/formula-empirica-molecular/
Fenômeno Físico
É aquele que não altera a natureza dos compostos que compõem o sistema. Não ocorre alteração na estrutura molecular das substâncias participantes:
Alguns exemplos: mudanças de estado físico (fusão, solidificação, vaporização, condensação e sublimação), expansão de um gás, acendimento de uma lâmpada.
Perceba que não há alteração na estrutura molecular: H2O(s) → H2O(ℓ) É t udo água, apenas mudando de Estado Sólido para Estado Líquido.
No exemplo, o derretimento de uma geleira – Fonte: meioambiente.culturamix.com
Dica 1 – Química Enem: Diagrama de fases. Entenda porque é possível patinar no gelo – https://blogdoenem.com.br/quimica-diagrama-de-fases/
Dica 2 – O que mais cai em Química nos Vestibulares e no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
Desafios
Questão 01
Um aluno, em uma aula prática de química, resolveu identificar dois sólidos (A e B) até então desconhecidos. Para isso ele fez uso de uma proveta, colocando 20 mL de água na mesma. Ao colocar o sólido A na proveta o volume aumentou para 25 mL. Repetiu então essa prática com o sólido B e de 20 mL, o volume de água na proveta aumentou para 30 mL. Pesando os sólidos A e B, ele obteve uma massa de 10 gramas do sólido A e 40 gramas com o sólido B. Com base nas experiências feitas, assinale a alternativa correta:
a) O sólido A é mais pesado que o sólido B;
b) O sólido B irá flutuar em um recipiente com água;
c) A densidade do sólido A é menor que a densidade do sólido B;
d) A e B apresentam a mesma massa;
e) A e B apresentam a mesma densidade.
Questão 02
A gasolina é vendida por litro, mas, em sua utilização como combustível, a massa é o que importa. Um aumento de temperatura do ambiente leva a um aumento no volume da gasolina. Para diminuir os efeitos práticos dessa variação, os tanques dos postos de gasolina são subterrâneos. Se os tanques não fossem subterrâneos:
I. Você levaria vantagem ao abastecer o carro na hora mais quente do dia, pois estaria comprando mais massa por litro de combustível.
II. Abastecendo com a temperatura mais baixa, você estaria comprando mais massa de combustível para cada litro.
III. Se a gasolina fosse vendida por kg em vez de por litro, o problema comercial decorrente da dilatação da gasolina estaria resolvido.
Das considerações, somente:
a) I é correta.
b) II é correta.
c) III é correta.
d) I e II são corretas.
e) II e III são corretas.
Questão 03
No processo de fabricação de pão, os padeiros, após prepararem a massa utilizando fermento biológico, separam uma porção de massa em forma de, “bola” e a mergulham num recipiente com água, aguardando que ela suba, como pode ser observado, respectivamente, em I e II do esquema abaixo. Quando isso acontece, a massa está pronta para ir ao forno.
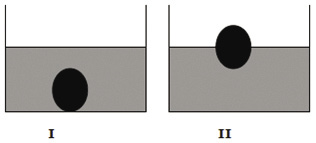
Um professor de Química explicaria esse procedimento da seguinte maneira:
“A bola da massa torna-se menos densa que o líquido e sobe. A alteração da densidade deve-se à fermentação, processo que pode ser resumido pela equação”:
C6H12O6 → C2H5OH + CO2 + Energia
Considere as afirmações abaixo:
I . A fermentação dos carboidratos da massa de pão ocorre de maneira espontânea e não depende da
existência de qualquer organismo vivo.
II. Durante a fermentação, ocorre produção de gás carbônico, que se vai acumulando em cavidades no interior da massa, o que faz a bola subir.
III. A fermentação transforma a glicose em álcool. Como o álcool tem maior densidade do que a água, a bola de massa sobe.
Dentre as afirmativas, apenas:
a) I está correta.
b) II está correta.
c) I e II estão corretas.
d) III está correta.
e) II e III estão corretas.
Questão 04
Pelas normas vigentes, o litro do álcool hidratado que abastece os veículos deve ser constituído de 96% de álcool puro e 4% de água (em volume). As densidades desses componentes são dadas na tabela.
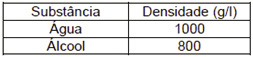
Um técnico de um órgão de defesa do consumidor inspecionou cinco postos suspeitos de venderem álcool hidratado fora das normas. Colheu uma amostra do produto em cada posto, mediu a densidade de cada uma, obtendo:
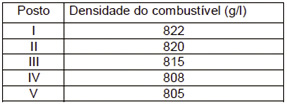
A partir desses dados, o técnico pôde concluir que estavam com o combustível adequado somente os postos:
a) I e II.
b) I e III.
c) II e IV.
d) III e V.
e) IV e V.
Questão 05
Produtos de limpeza, indevidamente guardados ou manipulados, estão entre as principais causas de acidentes domésticos. Leia o relato de uma pessoa que perdeu o olfato por ter misturado água sanitária, amoníaco e sabão em pó para limpar um banheiro:
A mistura ferveu e começou a sair uma fumaça asfixiante. Não conseguia respirar e meus olhos, nariz e garganta começaram a arder de maneira insuportável. Saí correndo à procura de uma janela aberta para poder voltar a respirar.
O trecho sublinhado poderia ser reescrito, em linguagem científica, da seguinte forma:
a) As substâncias químicas presentes nos produtos de limpeza evaporaram.
b) Com a mistura química, houve produção de uma solução aquosa asfixiante.
c) As substâncias sofreram transformações pelo contato com o oxigênio do ar.
d) Com a mistura, houve transformação química que produziu rapidamente gases tóxicos.
e) Com a mistura, houve transformação química, evidenciada pela dissolução de um sólido.
Você consegue resolver estes exercícios? Então resolva e coloque um comentário no post, logo abaixo, explicando o seu raciocínio e apontando a alternativa correta para cada questão. Quem compartilha a resolução de um exercício ganha em dobro: ensina e aprende ao mesmo tempo. Ensinar é uma das melhores formas de aprender!