Veja as Misturas Homogênas e as Misturas Heterogêneas para você entender o comportamento da água e do óleo. Resumo com aula gratuita de Química Enem.
Mistura é a junção de duas ou mais substâncias, sendo cada uma dessas denominadas de componentes. Mas, tem substâncias que se depender da natureza própria de cada uma delas não tem mistura. Confira nesta revisão de Química para Enem e vestibular.
Existem vários tipos de misturas e elas podem ser classificadas em: Mistura Homogênea e Mistura Heterogênea. Para que você entenda melhor as diferenças entre as misturas, é importante primeiro relembrar o conceito de fase, e o Blog do Enem não te deixa na mão. Vamos nessa!
Quando olharmos para uma amostra e conseguimos detectar uma porção uniforme, com características iguais em toda sua extensão, detectamos uma única fase. Pense em um copo contendo água do mar.
Embora saibamos que se trata de uma mistura, não percebemos qualquer diferença na amostra, ou seja, ela possui apenas uma fase.  Pense agora em um copo contendo água e óleo. Observe na imagem acima, ou faça uma experiência em casa. Eles não se misturam.
Pense agora em um copo contendo água e óleo. Observe na imagem acima, ou faça uma experiência em casa. Eles não se misturam.
Você sabe que eles não se misturam e facilmente identificamos uma porção com água e uma com óleo. Esse sistema (amostra) possui duas fases. Importante: Fases não estão ligadas ao estado físico. Você pode, como no exemplo da água e óleo, ter duas fases líquidas no mesmo sistema.
Agora vamos ver os tipos de misturas.
Misturas Homogêneas
São aquelas cujos componentes não conseguimos distinguir. Ela é perfeitamente uniforme, portanto monofásica.  O ar atmosférico e a água do mar são exemplos de misturas homogêneas. São exemplos de misturas homogêneas:
O ar atmosférico e a água do mar são exemplos de misturas homogêneas. São exemplos de misturas homogêneas:
Misturas heterogêneas
São aquelas formadas por mais de uma fase. Nelas conseguimos distinguir mais de um componente.  Água e óleo, ar e poeira, são exemplos de misturas heterogêneas.
Água e óleo, ar e poeira, são exemplos de misturas heterogêneas.
Mas, como você pode identificar uma mistura homogênea de uma substância pura? – É simples! A resposta para isso é a curva de aquecimento, que é o gráfico que mostra a variação de temperatura de uma amostra quando aquecida ou resfriada, incluindo-se as mudanças de estado físico.
Sabemos que durante uma mudança de estado físico a temperatura permanece constante e que, durante o aquecimento sem mudança de estado, sua variação é linear. Observe as curvas abaixo, de uma substância pura e de uma mistura homogênea.
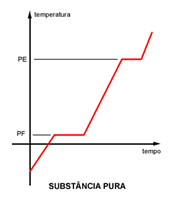 Curva de aquecimento de uma substância pura
Curva de aquecimento de uma substância pura
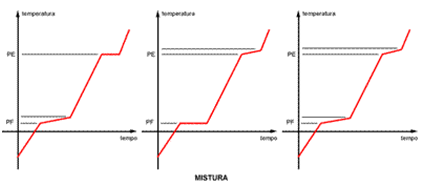 Curva de aquecimento de uma mistura homogênea
Curva de aquecimento de uma mistura homogênea
Você pode observar, no gráfico da mistura, que o patamar para a mudança de estado, ponto de fusão (PF) e ponto de ebulição (PE) não é constante, caracterizando uma mistura, já que para substâncias simples, a temperatura nessa etapa é constante.
Mistura Comum, Eutética e Azeotrópica, o que é? Preste atenção!
Quando a curva de aquecimento apresenta variação nos dois pontos (PF e PE), dizemos que é uma mistura comum. Quando um, e apenas um dos pontos apresenta variação, essa mistura receberá um nome especial.
- PF varia e PE constante: mistura azeotrópica
- PF constante e PE varia: mistura eutética
- Exemplos comuns dessas misturas são: água e álcool para mistura azeotrópica e gelo e sal de cozinha para mistura eutética.
Aprenda ainda mais sobre as misturas assistindo a este vídeo de Química do professor Sobis do Blog do Enem. Vamos lá! Não fique de fora dessa.
Dicas de Química do Blog do Enem
Dica 1– O que mais cai em Química nos Vestibulares no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
Dica 2– Saiba também como se faz a separação das misturas. Acesse o nosso Blog do Enem e fique sabendo de tudo! https://blogdoenem.com.br/quimica-separacao-misturas/
Dica 3 – Reveja também outro assunto bastante cobrado nas provas do Enem e dos vestibulares que é borrachas. Acesse o nosso blog do Enem e veja um super- resumo preparado pela professora Munique Dias. Vai ficar de fora dessa? https://blogdoenem.com.br/quimica-borrachas-naturais-sintetica/
Agora um desafio para você!
(Markenzie – SP) Água mineral engarrafada, propanona (C3H6O) e gás oxigênio são classificados, respectivamente, como:
- Substância pura composta, substância pura simples e mistura homogênea.
- Substância pura composta, mistura homogênea e substância pura simples.
- Mistura heterogênea, substância pura simples e substância pura simples.
- Mistura homogênea, substância pura composta e substância pura composta.
- Mistura homogênea, substância pura composta e substância pura simples.
Dica 4 – Relembre outros assuntos de química acessando o nosso blog www.blogdoenem.com.br e gabarite as questões de química nas provas dos vestibulares e do Enem.


