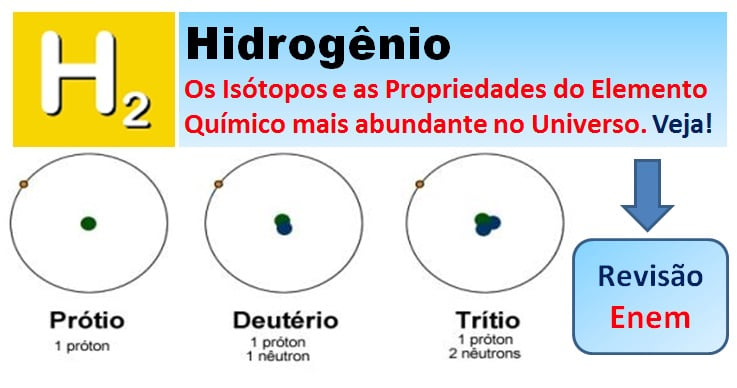
É hora de relembrar o essencial sobre um Elemento Químico da Tabela Periódica que é bastante estudado como futuro combustível limpo e fonte de energia: isso mesmo, com você, o Hidrogênio. Confira abaixo para gabaritar Química nas provas.
O hidrogênio possui a estrutura atômica mais simples que qualquer outro Elemento Químico da Tabela Periódica. O seu núcleo contém um próton com carga +1, com um elétron circundante e configuração eletrônica 1s¹.
Os átomos de hidrogênio podem alcançar a estabilidade de três maneiras diferentes:
- Formando uma ligação covalente (um par de elétrons) com outros átomos;
- Perdendo um elétron para formar H+;
- Adquirindo elétrons e formando H-;

Veja como o Hidrogênio foi descoberto:
- O alquimista Theophrastus Bombastus von Hohenheim, conhecido como “Paracelsus”, na manipulação de metais e ácidos produziu um ar explosivo ao qual ele inocentemente ignorava que fosse um elemento químico.
- Já em 1766, o químico Henry Cavendish identificou este gás como uma Sustância Química individual. Mas foi o francês Antoine Lavoisier que nomeou de Hidrogênio o elemento em 1783, e descobriu a também assim posteriormente a fórmula da água.
- O Hidrogênio é o elemento químico mais abundante no universo. Porém, na crosta terrestre é relativamente difícil de encontrar esse gás (H2).
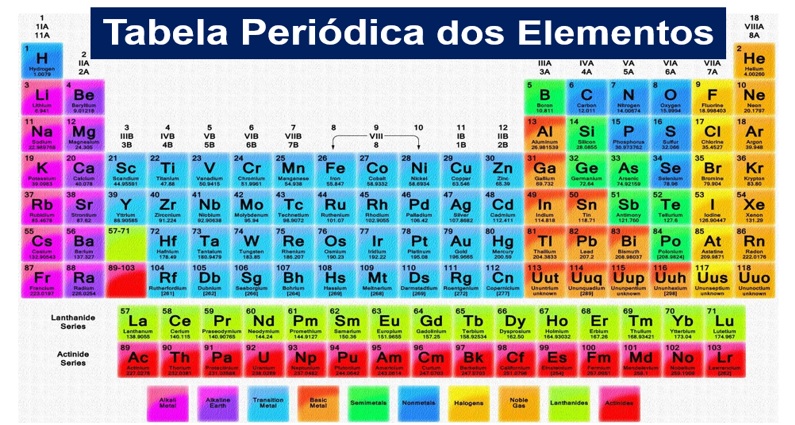
Veja a posição do hidrogênio na tabela periódica
O hidrogênio (H) é o primeiro elemento da Tabela Periódica, e apresenta características únicas. A estrutura eletrônica do átomo de hidrogênio se assemelha com a dos metais alcalinos (Grupo 1 da Tabela Periódica), com a dos halogênios e com os elementos do Grupo 14.
No caso da estrutura semelhante com metais alcalinos é devido à tendência muito maior que hidrogênio apresenta de formar ligações covalentes.
Já os halogênios geralmente adquirem elétrons formando íons negativos X-. Não é comum o hidrogênio formar um íon negativo, embora ele forme hidretos iônicos M+H- com alguns metais altamente eletropositivos, justificando sua semelhança com a estrutura eletrônica dos halogênios.
Em alguns aspectos, a estrutura eletrônica do hidrogênio também se parece com as dos elementos do Grupo 14, pois ambos possuem o nível externo semi-preenchido.
É hora de recordar a Tabela Periódica
Você lembra-se da tabela periódica e como ela é dividida? Que tal relembrar acessando o nosso blog do Enem e estudando através de um super-resumo que preparamos especialmente para você. Confira aqui a Tabela Periódica.
O quanto de Hidrogênio temos no universo:
O hidrogênio é o elemento mais abundante do universo. Segundo avaliações, o universo é constituído por 92% de hidrogênio e 7% de hélio, de modo que todos os demais elementos juntos representam apenas 1%. Entretanto, a quantidade de H2 na atmosfera terrestre é muito pequena, pois o campo gravitacional da terra é pequeno demais para reter um elemento tão leve.
Apesar disso, um pouco de H2 é encontrado nos gases vulcânicos. Em contrapartida, o hidrogênio é o décimo elemento mais abundante da crosta terrestre (1520 ppm ou 0,152 % em peso). Também é encontrado em grandes quantidades nas águas dos oceanos.
Compostos contendo hidrogênio são muito abundantes, sobretudo a água, organismos vivo (carboidratos e proteínas), compostos orgânicos, combustíveis fósseis (carvão, petróleo e gás natural), amônia e ácidos. De fato, o hidrogênio forma mais compostos que qualquer outro elemento.
Dica 1 – O que mais cai em Química nos Vestibulares e no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
Dica 2 –Quer relembrar sobre a evolução dos modelos atômicos? Então acesse o nosso Blog do Enem e confira um super-resumo que nós preparamos especialmente para você. Vamos lá! Faça a diferença! https://blogdoenem.com.br/quimica-atomo-khan-academy/
Dica 3 – Reações Químicas – Reveja também outro assunto de química que cai bastante nas provas dos vestibulares e do Enem que é Reações Químicas. Acesse o nosso blog do Enem e veja um super resumo preparado pela professora Munique Dias. Vai ficar de fora dessa?https://blogdoenem.com.br/quimica-reacoes-quimicas/
Aula Gratuita
Para fixar um pouco mais esse conteúdo assista ao vídeo sobre Hidrogênio mande bem nas questões de química dos vestibulares e também no Enem. Não deixe essa chance passar!
Os Isótopos de Hidrogênio
Isótopos são átomos de um mesmo elemento que possuem diferentes números de massa. A diferença nos números de massa decorre da quantidade diferente de nêutrons no núcleo. O hidrogênio encontrado na natureza é constituído por três isótopos: prótio 11H ou H, o deutério 21H ou D, e o trítio 31H ou T. Esses isótopos contem no núcleo 1 próton e zero, 1 ou 2 nêutrons, respectivamente. O prótio é o mais abundante.
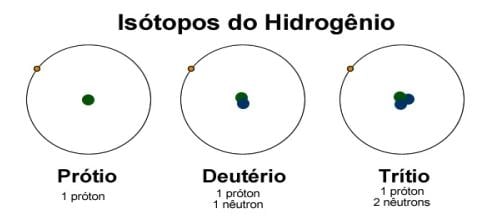
O hidrogênio encontrado na natureza contém 99,986% do isótopo 11H, 0,014% do isótopo 21H e 7 x10-16 % do isótopo 31H,de modo que as propriedades do hidrogênio são essencialmente devido ao isótopo mais leve.
Esses isótopos apresentam a mesma configuração eletrônica e essencialmente as mesmas propriedades químicas. As únicas diferenças são encontradas nas velocidades de reação e nas constantes de equilíbrio.
Você já deve ter ouvido falar no Hidrogênio como combustível e fonte de energia, vamos saber mais um pouco? Vem com a gente!
O hidrogênio como combustível e fonte de energia está sendo pesquisado em vários países do mundo, constituindo uma terceira geração de combustíveis cuja entrada em operação comercial é prevista para o pós-2030.
O hidrogênio apresenta algumas vantagens: traz benefícios ambientais (em sua combustão gera apenas vapor d’água como subproduto, e não compostos de carbono que causam emissões de gases de efeito estufa); e é um recurso ilimitado (que, combinado com o oxigênio, na forma de água, existe em grande quantidade).
Mas há algumas barreiras à expansão do uso do hidrogênio como combustível e fonte de energia: não se trata de um combustível primário (não é encontrado na natureza em estado puro, em quantidade significativa); há dificuldades em seu armazenamento para uso veicular (é um composto de baixíssima densidade, que ocupa muito volume, mas uma alternativa é o seu armazenamento na forma de hidretos, compostos instáveis que o liberam lentamente);
A produção de Hidrogênio a partir de recursos renováveis ainda não é economicamente competitiva; e as tecnologias para eliminação completa de carbono do ciclo produtivo ainda estão em desenvolvimento.As principais rotas hoje existentes para a produção do hidrogênio são reforma do gás natural ou de etanol; gaseificação de carvão ou biomassa; eletrólise da água; rotas fermentativas; e processos combinados, como energia solar associada à eletrólise.
O Hidrogênio como Fonte de Energia:
Assista mais um pouco sobre o Hidrogênio como fonte de energia por Matheus Prado e fique por dentro desse assunto. Fique ligado! Além de química isso é um assunto de atualidade, então fique por dentro!
Dica 4 -Relembre outros assuntos de química acessando o nosso blog www.blogdoenem.com.bre gabarite as questões de química nas provas dos vestibulares e do Enem