Você lembra como encontrar a proporção dos átomos em uma substância? E a sua fórmula molecular? Vamos relembrar Fórmula Empírica e Molecular. Aula da professora Munique Dias, de Química.
Olá, o cálculo da fórmula mínima e molecular de uma substância, não é um assunto muito dominado pelos alunos que realizam as provas do Enem e dos vestibulares. Mas fique tranquilo, o blog do Enem não te deixa na mão!
Nós preparamos um super-resumo para você, com videoaulas da Khan Academy e as explicações da professora Munique Dias. Não deixe essa chance passar! Acertar uma questão assim faz toda a diferença na sua nota final!
A análise da composição de uma substância desconhecida nos permite determinar quais elementos (análise qualitativa) que constituem a molécula e em qual proporção os átomos se encontram (análise quantitativa) na mesma. É possível fazermos uma análise quantitativa de uma substância através da sua fórmula empírica e molecular.
Mas o que é mesmo a fórmula molecular de uma substância? – A fórmula molecular nos indica o número de átomos de cada elemento que compõe a molécula ou espécie química da substância, bem como e proporção entre eles. Por exemplo: A molécula do peróxido de hidrogênio é formada por dois átomos de hidrogênio e dois átomos de oxigênio. Portanto e sua fórmula molecular é: H2O2 .
Mas como é possível calcular a fórmula molecular de uma substância? Para a determinação da fórmula molecular é necessário primeiro obter a fórmula empírica dessa mesma substância.
Ops! Fórmula empírica? Complicou agora? Que nada o blog do Enem esclarece para você.

A fórmula empírica (ou mínima) indica a proporção, em menores números inteiros, entre os átomos dos elementos que formam as substâncias.
Por exemplo: Na glicose (C6H12O6) a proporção dos átomos é de um átomo de carbono, para dois de hidrogênio, para um de oxigênio, ou seja, CH2O (1:2:1).
É importante salientar que este tipo de fórmula não é suficiente para identificar uma substância. Há casos em que a fórmula mínima de uma substância corresponde à fórmula molecular de outra. E há substâncias que podem apresentar a mesma fórmula mínima.
Confira neste quadro:
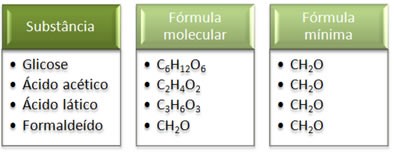
Veja que a fórmula mínima CH2O é a mesma para todas as substâncias, isto é, ela expressa que, em todos os casos, os átomos de carbono, hidrogênio e oxigênio estão presentes nas fórmulas moleculares em uma relação de 1:2:1. Além disso, o único que apresenta a fórmula molecular igual à fórmula empírica é o formaldeído.
Complicou? Assista a vídeoaula do Curso Enem Gratuito e fique fera neste assunto!

Dica 1 – Não lembra o que é fórmula percentua? Acesse o link: http://www.brasilescola.com/quimica/formula-percentual-ou-centesimal.htm e não fique com dúvidas!
Quer ver exemplos ? Assista agora a uma super videoaula de exercícios e explicações da Khan Academy com o professor Salman Khan e fique fera!
Determine a fórmula molecular de um óxido de fósforo que apresenta 43,6% de fósforo e 56,4% de oxigênio (porcentagem em massa) e massa molar 284 (massas atômicas: P = 31; O = 16).
Resposta: P4O10 .