Você lembra como identificar o número atômico e número de massa de um átomo? Que tal relembrar e tirar de letra na prova do Enem e nos vestibulares de todo Brasil? O Blog do Enem te ajuda nessa, estude com a gente!
Química Enem: O modelo atual do átomo é baseado no de Rutherford (chamado modelo planetário ou Sistema Solar), e segundo ele duas regiões formariam o átomo: um núcleo pequeno positivo e de alta densidade, e uma região extranuclear (a eletrosfera), que seria como um espaço vazio em que estão distribuídos os elétrons.
Rutherford deu uma grande contribuição para a ciência quando em 1914 demonstrou a existência de uma partícula de massa bem maior do que a do elétron, mas de sinal oposto (isto é, positivo), que em 1920 recebeu o nome de prótons.
Em 1932, o físico inglês James Chadwick descobriu uma partícula com aproximadamente a mesma massa do próton, mas que não era carregada eletricamente, e por esse motivo chamada de Nêutron.

Assim, foram definidos alguns conceitos diretamente relacionados a essas partículas, suas cargas e seus números, que servem para identificar os átomos, como o número de massa (A) e o número atômico (Z).
Dica 1– O que mais cai em Química nos Vestibulares no Enem? Veja aqui as melhores dicas: https://blogdoenem.com.br/enem-2013-quimica-cai-mais/
O número atômico (Z) é a quantidade de prótons presente no núcleo do átomo.
Cada elemento químico possui um número atômico, ou seja, não existem átomos de elementos químicos distintos que apresentem o mesmo número atômico; por isso, os números atômicos dos elementos facilitam a classificação e a constituição da tabela periódica.
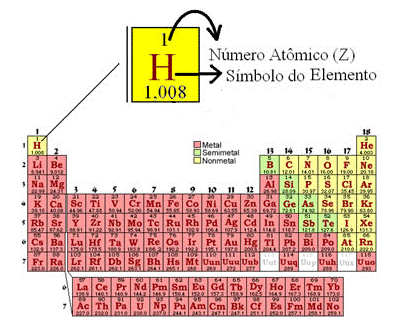
Observando os elementos na Tabela Periódica, o número atômico (Z) vem em cima do respectivo elemento, indicando quantos prótons ele tem no núcleo.
Dica 2– Você acha difícil memorizar tudo que aprende? O Blog do Enem pode te ajudar! Acesse o link e descubra quais as dicas para você memorizar o que estudou: https://www.alunosonline.com.br/portugues/dicas-para-voce-memorizar-o-que-estuda.html
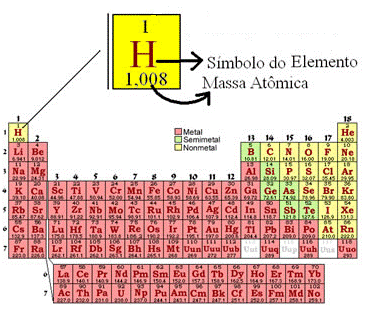
O número de massa (A) é a soma do número de prótons ou número atômico com o número de nêutrons existentes no núcleo.
Ou seja:
A= Z + n
Ou se você possuir o número de massa e precisa encontrar o número de nêutrons:
n= A – Z
Dica 3 – Reveja também outro assunto bastante cobrado nas provas do Enem e dos vestibulares que é o histórico da química orgânica. Acesse o nosso blog do Enem e veja um super- resumo preparado pela professora Munique Dias. Vai ficar de fora dessa? https://blogdoenem.com.br/historico-da-quimica-organica-revisao-para-o-enem-e-vestibular/
Que tal reforçar esse assunto e mandar bem nas provas dos vestibulares e do Enem? Em menos de 10 minutos você pode rever tudo sobre a tabela periódica e estudar ainda mais! Não deixe de conferir!
Você consegue resolver este exercício? Então resolva e coloque um comentário no post, logo abaixo, explicando o seu raciocínio e apontando a alternativa correta para questão. Quem compartilha a resolução de um exercício ganha em dobro: ensina e aprende ao mesmo tempo. Ensinar é uma das melhores formas de aprender!
O átomo de um elemento químico possui 83 prótons, 83 elétrons e 126 nêutrons. Qual é, respectivamente, o número atômico e o número de massa desse átomo?
a) 83 e 209.
b) 83 e 43.
c) 83 e 83.
d) 209 e 83.
e) 43 e 83.
Resposta: a
Dica 4 – Relembre outros assuntos de química acessando o nosso blog www.blogdoenem.com.br e gabarite as questões de química nas provas dos vestibulares e do Enem.










