A isomeria espacial geométrica só pode ser identificada por meio da consideração da disposição dos átomos da molécula no espaço. Veja este super resumo com aula gratuita, exemplos e imagens bem legais para você compreender o fenômeno. É para gabaritar em Química. Vem!
Hora de relembrar tudo sobre isomeria geométrica e mandar super bem na prova do Enem e dos vestibulares de todo Brasil. A isomeria geométrica ocorre especialmente em compostos de cadeia aberta que possuem ligação dupla entre pelo menos dois átomos de carbono, sendo que cada átomo de carbono da dupla possui os seus grupos ligados diferentes entre si.
Esse tipo de isomeria é também denominada de estereoisomeria e os isômeros de estereoisomeros.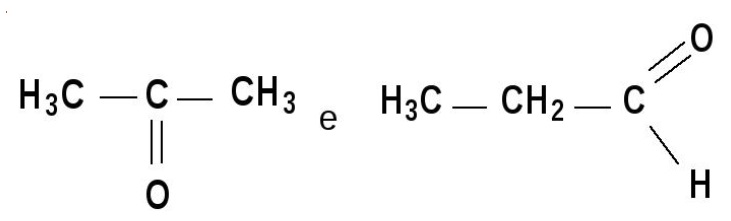 Não é possível ver a diferença entre esses isômeros somente analisando a fórmula estrutural plana, porque eles possuem o mesmo tipo de cadeia carbônica, o mesmo grupo funcional, a mesma insaturação e o mesmo substituinte ou heteroátomo.
Não é possível ver a diferença entre esses isômeros somente analisando a fórmula estrutural plana, porque eles possuem o mesmo tipo de cadeia carbônica, o mesmo grupo funcional, a mesma insaturação e o mesmo substituinte ou heteroátomo.
A isomeria espacial geométrica só pode ser identificada por meio da consideração da disposição dos átomos da molécula no espaço.
Resumo de Isomeria Geométrica
Veja um resumo simples e rápido com a professora Larissa campos, do canal do Curso Enem Gratuito:
Muito bom o resumo.
Conseguiu entender? Vamos ver um exemplo para ficar mais fácil…
Observe os dois isômeros formados pelo but-2-eno: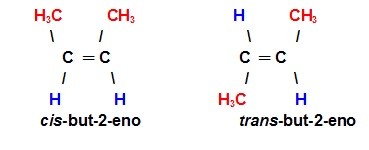 Figura 1. Isômeros do but-2-eno
Figura 1. Isômeros do but-2-eno
Na primeira molécula, os ligantes iguais estão do mesmo lado do plano espacial, por isso esse isômero é chamado de CIS. Na outra molécula, os ligantes iguais estão em lados opostos do plano, portanto, são chamados de TRANS.
Então, … resumindo...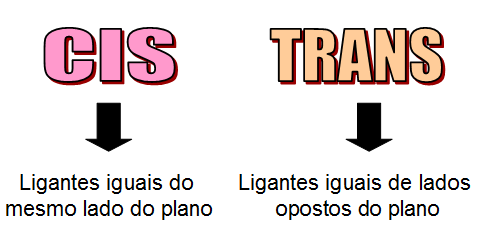 Você deve estar pensando, porque a isomeria geométrica só ocorre em compostos de carbono com ligação dupla? Calma! O blog do Enem te ajuda a entender.
Você deve estar pensando, porque a isomeria geométrica só ocorre em compostos de carbono com ligação dupla? Calma! O blog do Enem te ajuda a entender.
Entenda a dupla ligação:
É que a dupla ligação entre os carbonos é rígida, ou seja, não é passível de sofrer rotação e de ser a mesma molécula, correspondendo assim, a compostos diferentes.
É por isso que a isomeria geométrica não ocorre em compostos de cadeia aberta que sejam saturados, isto é, que possuam somente ligações simples entre os carbonos, tendo em vista que essas ligações podem sofrer rotação transformando-se assim, na mesma molécula.
Já nas ligações triplas entre os carbonos, a isomeria geométrica também não ocorre, porque tais átomos só podem realizar mais uma ligação, visto que já possuem três.
A diferença na estrutura dos isômeros pode até parecer pouca coisa, porém, representa uma grande diferença nas características físicas e químicas desses isômeros.
Por exemplo, pegando o 1,2-dicloro-etileno, veja no quadro abaixo os diferentes pontos de ebulição, de fusão e de densidade de cada um: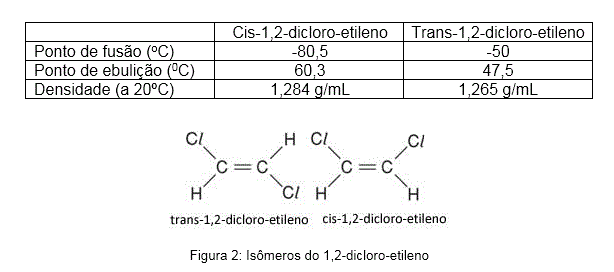
Isomeria Plana – Veja todos os tipos
Confira agora com a professora Larissa Campos, do cnaal do Curso Enem Gratuito, todos os tipos de Isomeria para você mandar bem nas questões de Química do Enem:
Dica – Reveja também outro assunto bastante cobrado nas provas do Enem e dos vestibulares: as fórmulas químicas. Acesse o nosso blog do Enem e veja um super-resumo preparado pela professora Munique Dias. Vai ficar de fora dessa?
Resumo final de Isomeria
o professor Felipe Sobis, do canal Curso Enem Gratuito. Vai ajudar você a compreender.
Exercício de Isomeria
Você consegue resolver este exercício sobre isomeria geométrica? Então resolva e coloque um comentário no post, logo abaixo, explicando o seu raciocínio e apontando a alternativa correta para questão. Quem compartilha a resolução de um exercício ganha em dobro: ensina e aprende ao mesmo tempo. Ensinar é uma das melhores formas de aprender!
(UEPB) Inúmeros exemplos de substâncias naturais apresentam o fenômeno da isomeria geométrica. Dentre estas, os ferormônios – substâncias que alguns insetos utilizam para se comunicar, e com isso, demarcar territórios, dar alarmes ou atrair outros insetos na época de acasalamento. Atualmente, os cientistas estão tentando criar armadilhas com feromônios sexuais com o intuito de atrair os machos (exemplo da mosca doméstica), impedindo dessa forma a propagação de doenças. Foi observado, no entanto, que o macho da mosca caseira só é atraído pelo isômero cis. O trans não causa o menor efeito nesse fenômeno de atração sexual.
Dados os compostos abaixo:
I. 2-penteno
II. 1-penteno
III. ciclobutano
IV. pentano
Assinale a alternativa que corresponde aos compostos que apresentam isomeria (cis-trans):
a) Apenas III.
b) Apenas I e II.
c) Apenas II e IV.
d) Apenas I
e) I, II, III e IV
Resposta: d


